黑色素瘤细胞分泌的黑素体携带主要组织相容性复合体分子和肿瘤抗原,通过结合CD8+T细胞的T细胞受体诱发其功能障碍与凋亡,助力肿瘤免疫逃逸,抑制黑素体分泌可显著增强抗肿瘤免疫效果。
皮肤癌中,黑色素瘤以每年10万新增病例的规模成为致命威胁。尽管免疫治疗为部分患者带来希望,但仍有近半数患者对治疗无应答,即便肿瘤表达能被免疫细胞识别的突变抗原,负责杀伤肿瘤的CD8+T细胞也难以发挥作用。
近期,发表于Cell的一项颠覆性研究揭开了黑色素瘤的隐身绝技,肿瘤细胞分泌的黑素体,竟能化身“免疫陷阱”,让本应杀伤肿瘤的CD8+T细胞失去战斗力。这一发现为攻克免疫治疗耐药提供了全新方向。
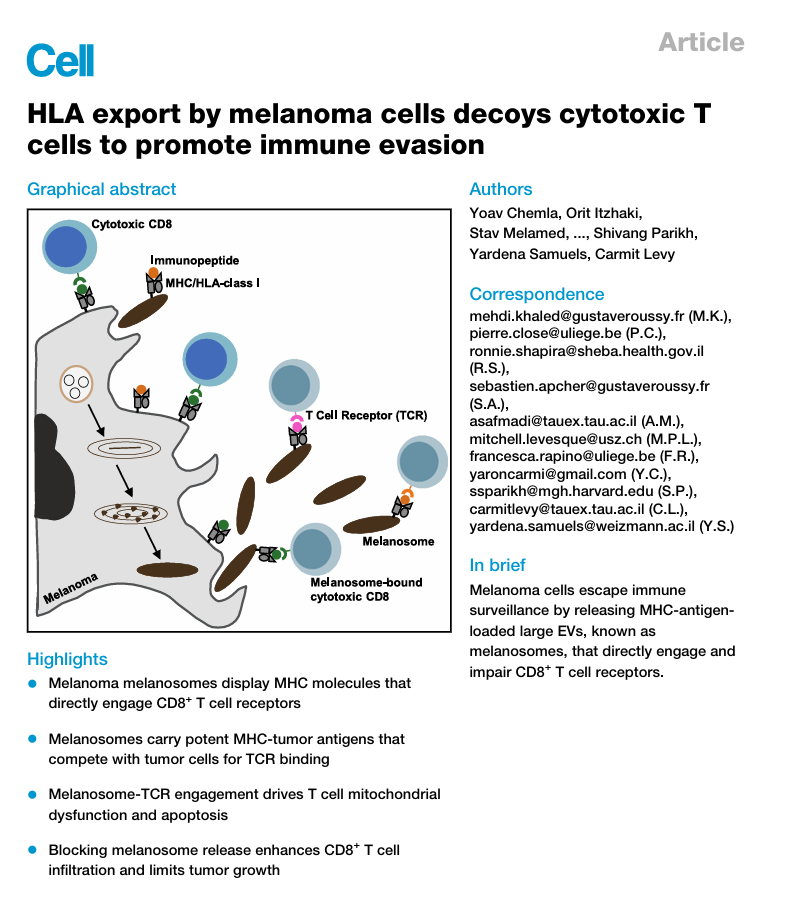
黑素体存在与否直接关联治疗效果与预后
研究通过分析TCGA数据库和69例转移性黑色素瘤患者样本发现,黑素体相关基因高表达的患者,复发风险更高、生存期更短。免疫治疗无应答者体内,负载色素的T细胞数量显著多于应答者,且这些T细胞体积更小,呈现典型的功能耗竭特征。
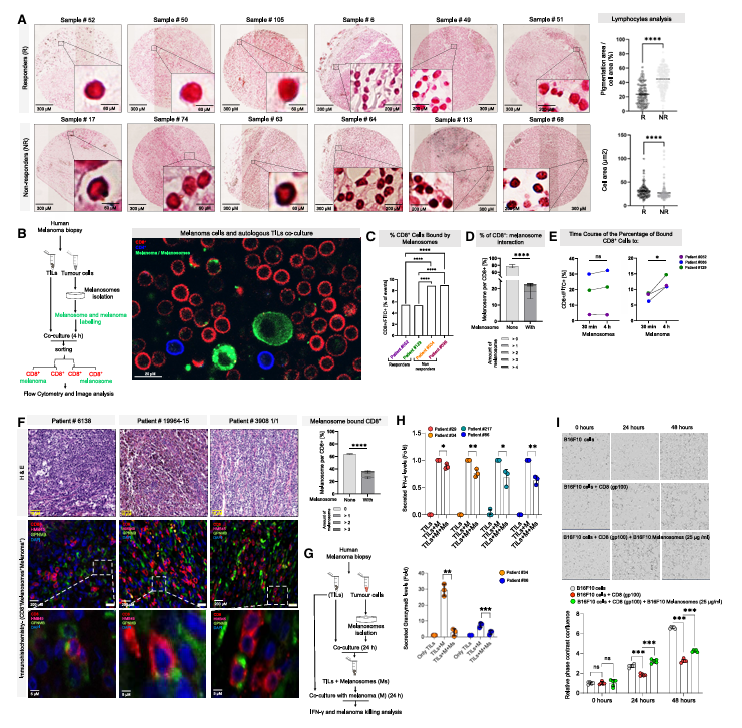
图1:黑素体的存在与不良预后、免疫治疗无应答及T细胞细胞毒性降低相关
进一步实验证实,黑素体与CD8+T细胞的结合效率极高,30分钟内即可完成结合并稳定维持4小时以上,一个黑色素瘤细胞每天可分泌约40个黑素体。当肿瘤浸润淋巴细胞预暴露于黑素体后,干扰素γ和颗粒酶B的分泌量大幅减少,对肿瘤细胞的杀伤能力明显下降。
抑制黑素体分泌可打破肿瘤生长魔咒
为验证黑素体的作用,研究人员使用脱色素剂曲酸抑制酪氨酸酶活性,从而减少黑素体分泌。实验显示,曲酸不会影响肿瘤细胞增殖或CD8+T细胞的存活,却能特异性降低黑色素瘤的色素沉着和黑素体释放。
在小鼠黑色素瘤模型中,曲酸治疗让肿瘤生长明显受限,小鼠生存期显著延长,肿瘤组织中CD8+T细胞的浸润量大幅增加。而当使用抗体耗竭CD8+T细胞后,曲酸的抗肿瘤效果被削弱,证实其作用依赖CD8+T细胞。此外,CRISPR-Cas9敲除酪氨酸酶的黑色素瘤细胞,也呈现出类似的抗肿瘤表型,进一步验证了黑素体在肿瘤进展中的关键作用。
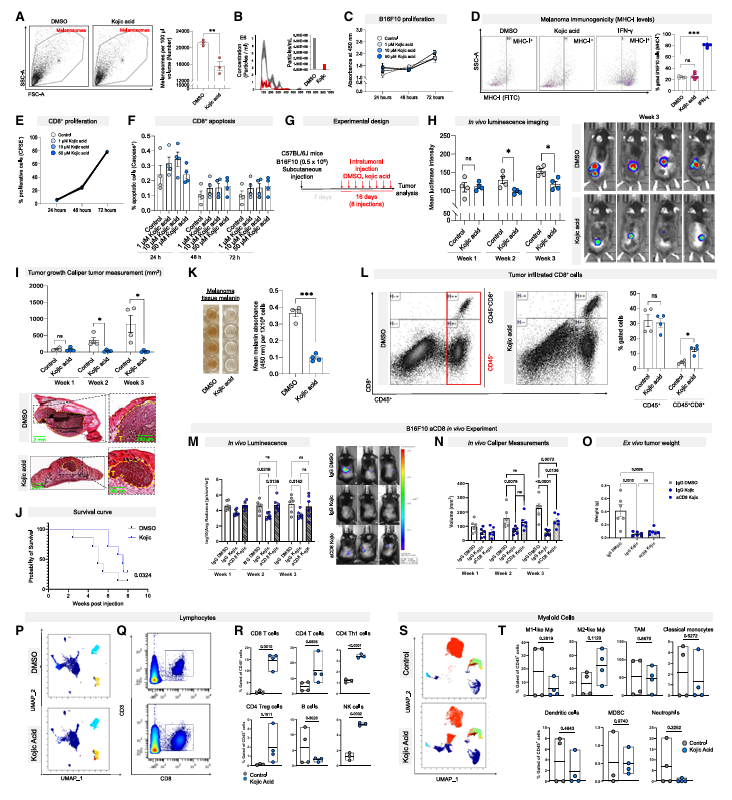
图2:抑制黑色素瘤细胞的黑素体分泌可阻断肿瘤进展并诱导CD8+T细胞浸润
MHC-TCR结合:黑素体“捕获”T细胞的核心机制
蛋白质组学分析显示,与外泌体不同,黑色素瘤来源的黑素体富含免疫相关蛋白,尤其是MHC I类分子(人类为HLA分子)。这些MHC I类分子能正确负载肿瘤抗原肽,具备与T细胞受体(TCR)结合的能力。
电子显微镜观察发现,黑素体与CD8+T细胞形成类似免疫突触的膜对膜接触,且这种结合具有抗原特异性——仅携带对应抗原的黑素体能与表达特异性TCR的CD8+T细胞结合。当黑素体缺乏MHC I类分子时,其与CD8+T细胞的相互作用显著减弱,证明MHC-肽-TCR相互作用是结合的核心机制。
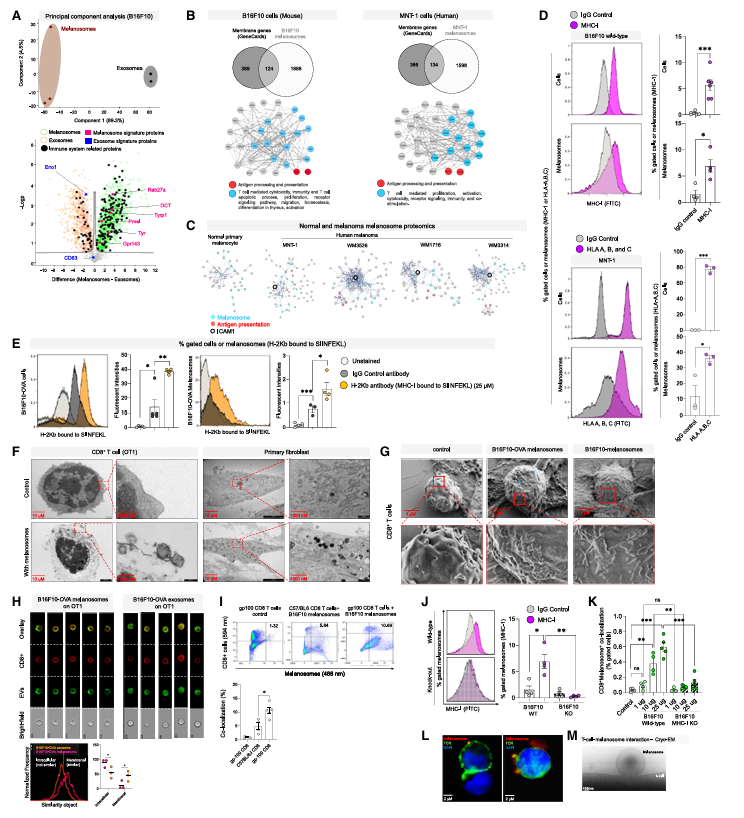
图3:黑素体膜上的MHC I类分子与CD8+T细胞上的T细胞受体结合
黑素体携带高免疫原性抗原,与肿瘤细胞“争夺”T细胞
免疫肽组学分析显示,黑素体携带的MHC结合肽与肿瘤细胞表面肽段有83.8%的重叠,但黑素体上的肽段具有更高的MHC结合亲和力和疏水性,免疫原性更强。研究共在黑素体中鉴定出25种肿瘤相关抗原,且这些抗原在黑素体中的表达水平显著高于肿瘤细胞,同时还发现了3种突变衍生的新抗原。
TCR测序结果表明,黑素体结合的CD8+T细胞与肿瘤细胞结合的CD8+T细胞共享大量TCR克隆型。在免疫治疗无应答者中,肿瘤细胞特异性的TCR克隆比例显著降低,提示黑素体与肿瘤细胞竞争结合CD8+T细胞,成为T细胞与肿瘤细胞之间的物理屏障。
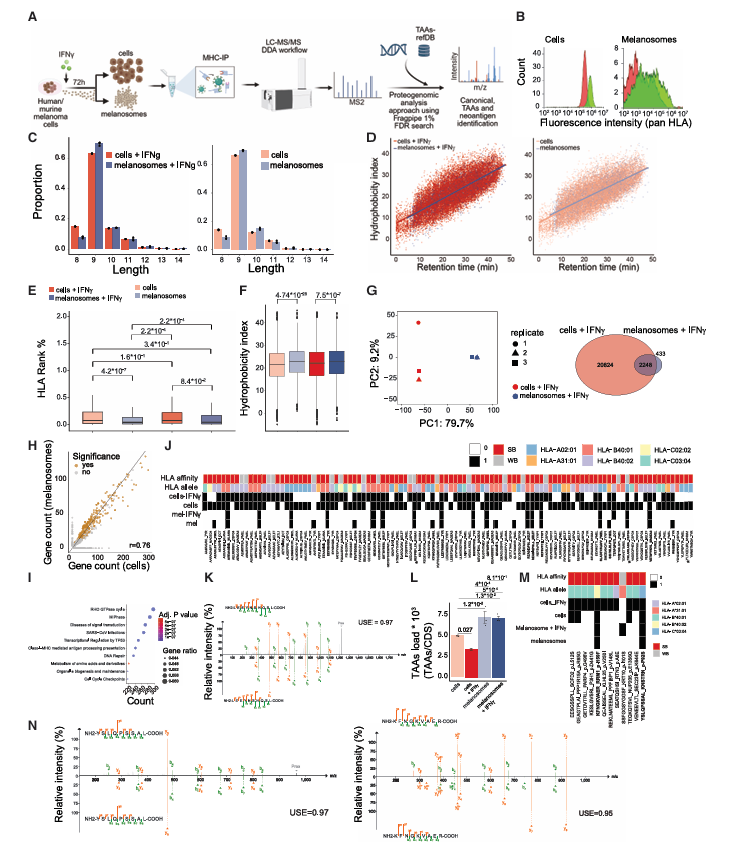
图4:人黑色素瘤黑素体的MHC免疫肽组分析显示黑素体携带肿瘤相关抗原和新抗原
黑素体诱导T细胞“功能紊乱”并凋亡
单细胞RNA测序显示,黑素体结合的CD8+T细胞呈现独特的转录特征:上调抗凋亡、黏附及炎症相关基因,下调增殖相关基因。尽管这些细胞的干扰素γmRNA水平略有升高,但TCR信号通路显著受抑,ZAP70磷酸化(TCR激活标志物)缺失,线粒体功能下降,呈现“功能紊乱”状态。
最终,黑素体结合会导致CD8+T细胞凋亡增加,且未诱导PD1、TIM3等经典耗竭标志物的表达,表明这是一种全新的T细胞功能抑制机制。
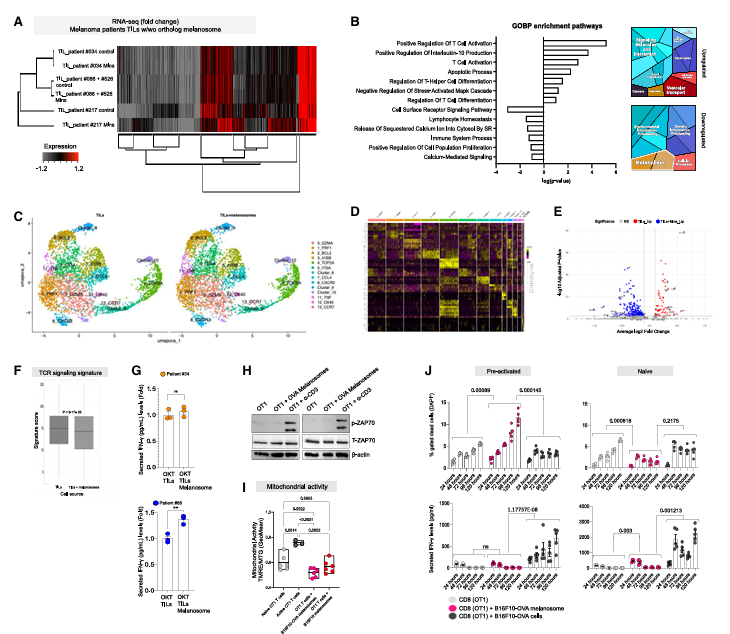
图5:黑素体与CD8+T细胞结合可诱导非最佳转录谱、降低T细胞受体信号传导和线粒体活性并导致凋亡
综上,这项研究首次完整揭示了黑色素瘤通过黑素体实现免疫逃逸的全新机制:黑素体作为肿瘤细胞分泌的“免疫诱饵”,携带MHC分子和高免疫原性抗原,与CD8+T细胞的TCR结合,诱导其功能障碍和凋亡,从而帮助肿瘤躲过免疫系统的攻击。
这一发现为黑色素瘤治疗提供了新的靶点。通过曲酸等药物抑制黑素体分泌,或开发针对黑素体形成、分泌相关通路的抑制剂,有望打破免疫治疗耐药,增强CD8+T细胞的抗肿瘤活性。未来,这类药物与免疫检查点抑制剂、过继性T细胞治疗等联合使用,可能为更多黑色素瘤患者带来治愈希望。
随着对黑素体介导免疫逃逸机制的深入探索,我们有望开发出更精准、更有效的治疗策略,让曾经“顽固”的黑色素瘤不再难治,为肿瘤免疫治疗领域注入新的活力。(生物谷Bioon.com)
参考文献:
Chemla Y, Itzhaki O, Melamed S, et al. HLA export by melanoma cells decoys cytotoxic T cells to promote immune evasion. Cell. Published online December 15, 2025. doi:10.1016/j.cell.2025.11.020
版权声明
本网站所有注明“来源:生物谷”或“来源:bioon”的文字、图片和音视频资料,版权均属于生物谷网站所有。非经授权,任何媒体、网站或个人不得转载,否则将追究法律责任。取得书面授权转载时,须注明“来源:生物谷”。其它来源的文章系转载文章,本网所有转载文章系出于传递更多信息之目的,转载内容不代表本站立场。不希望被转载的媒体或个人可与我们联系,我们将立即进行删除处理。
 NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站
NGS杂交捕获DNA探针 QuarStar 94基因泛肿瘤Panel 3.0 QuarStar 176基因泛肿瘤Panel 3.0 QuarStar 227基因融合Panel 1.0 QuarStar 515基因泛肿瘤Panel 1.0 杂交捕获RNA探针 人全外显子组探针3.0 HRD panel 建库试剂 DNA建库试剂盒 片段化试剂 磁珠法捕获mRNA试剂盒 rRNA去除试剂盒 QuarPro T4连接酶 杂交捕获试剂 DNA探针快速杂交捕获试剂 DNA探针杂交捕获试剂V2版 DNA探针杂交捕获试剂 RNA探针一管式过夜杂交试剂 RNA探针快速杂交捕获试剂 接头体系 封闭液系统 扩增子NGS BRCA超多重引物 超多重PCR试剂盒2.0 PathoSeq 450病原库 配套试剂 链霉亲和素磁珠 设备与软件 iQuars 50自动化工作站 RNA合成sgRNA miRNA siRNA
RNA合成sgRNA miRNA siRNA



 引物与探针
引物与探针 基因合成
基因合成 寡核苷酸池
寡核苷酸池 CRISPR sgRNA定制文库
CRISPR sgRNA定制文库 抗体库
抗体库 突变体库
突变体库








 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱: 电话:400-800-8820
电话:400-800-8820 地址:苏州市高新区88号
地址:苏州市高新区88号 邮箱:
邮箱:







